Dysréflexie autonome
Qu’est-ce que la dysréflexie autonome ?
Le système nerveux est un réseau complexe composé de plusieurs parties et sous-ensembles. L’une de ces parties est le système nerveux autonome (SNA) qui contrôle toutes les fonctions corporelles que vous ne pensez pas à provoquer. Le SNA équilibre le système nerveux sympathique et parasympathique. Le système nerveux autonome sympathique (SNAS) accélère les réactions corporelles tandis que le système nerveux autonome parasympathique (SNAP) ralentit ces réactions. Cette combinaison maintient le fonctionnement du corps en harmonie. Lorsqu’il est menacé, le système nerveux sympathique accélère sans être contenu par le système parasympathique, ce qui entraîne une réaction de « combat ou de fuite ». Si le corps est menacé, une libération d’énergie éclate à travers le système nerveux en réaction. C’est la réponse humaine habituelle à une menace.
Comparaisons de certaines des fonctions des systèmes nerveux sympathique et parasympathique :
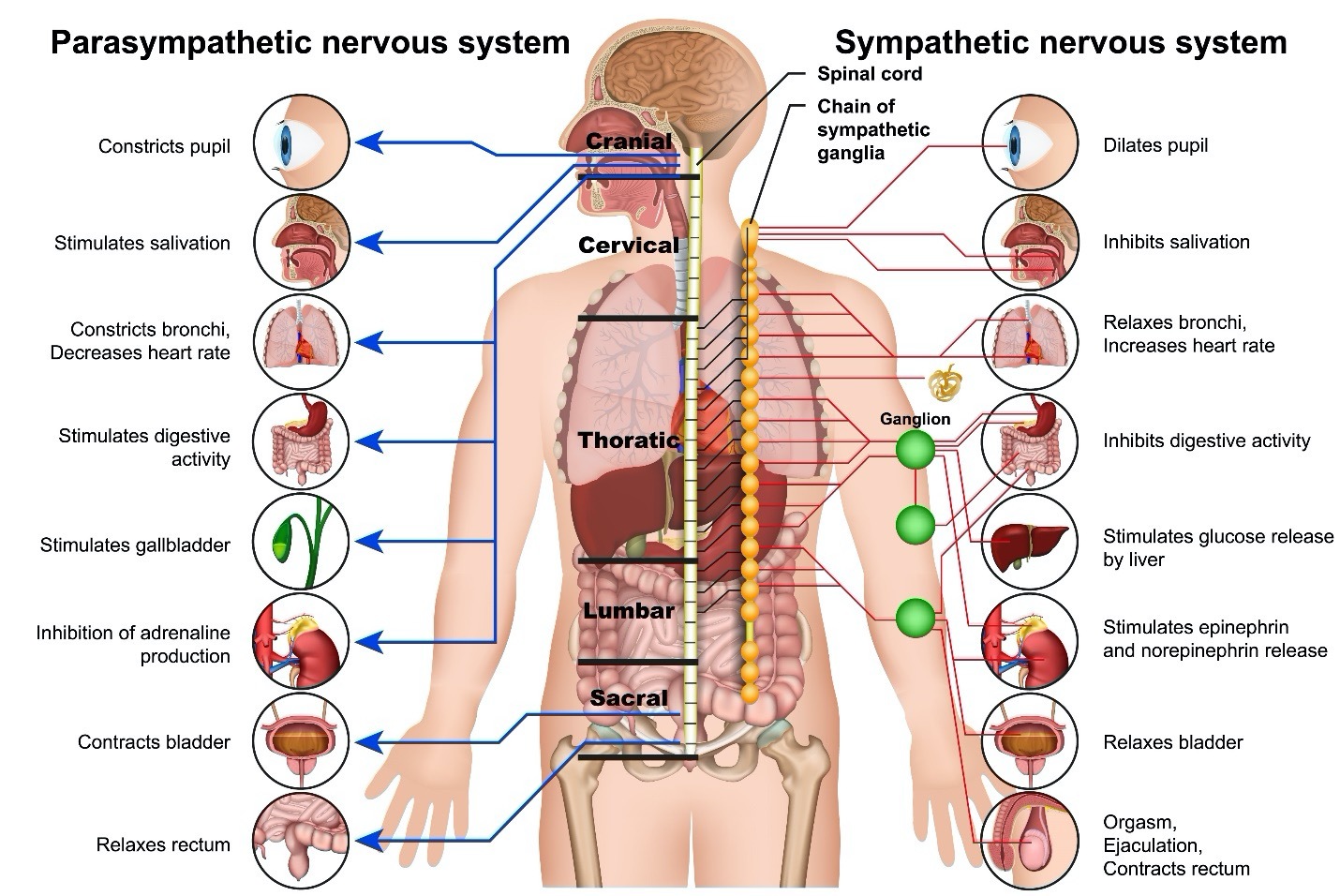
La dysréflexie autonome (DA) est un problème du système nerveux autonome. Les termes anciens pour la DA que l’on peut encore entendre aujourd’hui sont la dysautonomie et l’hyperréflexie parce qu’il y a trop de réponse (hyper)réflexique. Le système nerveux autonome (SNA) est la partie du système nerveux qui contrôle l’activité du corps sans que vous y pensiez consciemment. C’est ce qui permet au corps de fonctionner afin que vous puissiez vous concentrer sur d’autres choses.
Tout ce qui se produit dans votre corps et qui se produit automatiquement (ou sans que ce soit vous qui le contrôliez) est géré par le système nerveux autonome. Ces activités corporelles comprennent des centaines d’activités telles que les battements cardiaques, la respiration, la digestion, la régulation de la pression artérielle, le contrôle de la température corporelle, la réponse aux infections, la transpiration, les démangeaisons, le contrôle de la douleur, la détente des muscles, l’excitation sexuelle et la liste est encore longue. Chaque fonction de votre corps qui fonctionne sans pensée consciente est contrôlée par le système nerveux autonome.
Quand le système nerveux n’est pas endommagé, le corps perçoit des stimulations nocives ou désagréables à travers les nerfs sensoriels du corps. Ces nerfs envoient ensuite une impulsion au cerveau signalant le problème et donnant des détails sur l’emplacement. Le cerveau interprète le signal et envoie une réponse appropriée à travers les nerfs moteurs pour bouger, tourner, gratter, ajuster la température du corps, contrôler la pression artérielle ou, d’une manière ou d’une autre, adapter le corps.
Les nerfs moteurs contrôlent tous les mouvements du corps. Le mouvement comprend le déplacement de vos muscles pour permettre à vos bras et à vos jambes de fonctionner, mais aussi pour ajuster la température et la pression artérielle ainsi que le fonctionnement interne du corps. Dans le cerveau se trouvent les motoneurones supérieurs (cellules nerveuses) dont l’axone ou le bras atteint principalement la moelle épinière supérieure. Les interneurones relient les motoneurones supérieurs et inférieurs dans la moelle épinière. La moelle épinière est l’emplacement des neurones moteurs inférieurs (nerfs) dont l’axone ou le bras quitte le canal rachidien et s’étend dans le corps lui-même.
Une blessure qui affecte les motoneurones supérieurs produit une dysréflexie autonome (DA). Par conséquent, les personnes atteintes d’une lésion de la moelle épinière dans les régions cervicales ou thoraciques de la moelle épinière (au-dessus de T6) sont à risque de DA car c’est l’emplacement des axones ou des bras des motoneurones supérieurs. Sont également à risque les personnes atteintes de lésions cérébrales, d’accidents vasculaires cérébraux et d’autres maladies neurologiques si les motoneurones supérieurs du cerveau ou de la moelle épinière supérieure sont touchés.
Après une lésion du système nerveux, les communications vers et depuis le cerveau peuvent être des messages partiels, absents ou mal interprétés. Cependant, des messages sont toujours envoyés et reçus par les nerfs du SNA. Les nerfs sont dans tout le corps, y compris la zone de lésion. Votre système nerveux automatique fonctionne toujours mais peut-être pas au même niveau qu’avant votre lésion. Au lieu d’une petite réponse à un problème spécifique, une explosion d’énergie du système nerveux sympathique est libérée constituant une correction radicale. Le système nerveux parasympathique est incapable de ralentir la libération. Il s’agit d’une dysréflexie autonome, une sur-réponse réflexe automatique qui ne peut être contenue. Parce que le SNA est contrôlé automatiquement, vous ne pouvez pas consciemment modifier ou contrôler la réponse de dysréflexie autonome de votre corps. Un traitement d’urgence doit être mis en place immédiatement.
Personnes à risque de dysréflexie autonome
Les personnes souffrant de lésions causées par une maladie ou un traumatisme des nerfs moteurs supérieurs sont à risque de dysréflexie autonome. Traditionnellement, la présence d’une lésion de la moelle épinière au-dessus de T6 est le facteur déterminant de la DA, mais des recherches récentes indiquent que les personnes ayant subi une lésion à T10 et au-dessus ont signalé des symptômes.
Les personnes atteintes d’autres lésions affectant les motoneurones supérieurs ont également un risque de DA. Il s’agit notamment de personnes ayant reçu un diagnostic de lésion cérébrale, d’accident vasculaire cérébral, de sclérose en plaques, de syndrome de Guillain-Barré ou d’autres maladies neurologiques. Toute maladie ou lésion affectant le système nerveux autonome peut entraîner des épisodes de dysréflexie autonome. Un type particulier de perturbation autonome après une lésion cérébrale est l’hyperactivité sympathique paroxystique (PSH) qui se manifeste par une fièvre passagère, une tachycardie (fréquence cardiaque rapide), une hypertension (pression artérielle élevée), une tachypnée (respiration rapide), une transpiration excessive (transpiration), et des postures spécifiques. Être diagnostiqué de l’une des affections neurologiques énumérées ci-dessus ne signifie pas que vous développerez la DA. On ne comprend pas pourquoi certaines personnes développent la DA alors que d’autres ne le font pas. On ne comprend pas non plus pourquoi certains ont des symptômes plus graves que d’autres. Il existe de rares cas de personnes atteintes de DA sans diagnostic neurologique ou sans qu’on en connaisse la cause spécifique.
Symptômes de la dysréflexie autonome (DA)
Les caractéristiques des symptômes de la DA varient selon les individus. Certaines personnes présentent des symptômes extrêmement bénins qui sont malheureusement souvent ignorés. D’autres présentent des symptômes invalidants. Veuillez noter qu’avec une DA, vous pouvez présenter certains, quelques-uns ou tous les symptômes de la DA. Certains symptômes apparaîtront avec différents facteurs déclenchants. La plupart des individus apprennent que le mal de tête violent est un symptôme de la DA. Un mal de tête battant est le symptôme le plus souvent cité, mais n’importe lequel des symptômes énumérés peut être noté même en l’absence d’un mal de tête battant. Ignorer tout symptôme peut mettre la vie en danger, même s’il est léger. La surveillance de la pression artérielle est essentielle pour détecter la DA. Une pression artérielle élevée au-dessus de votre plage normale peut entraîner un accident vasculaire cérébral, un arrêt cardiaque, des convulsions, une hémorragie rétinienne, un œdème pulmonaire et même la mort si elle n’est pas traitée.
Les symptômes typiques de la DA chez l’adulte sont :
AU-DESSUS DU NIVEAU DE LESION
- Hypertension (une augmentation rapide de la pression artérielle, 20-40 mm Hg systolique plus élevée que d’habitude)
- Bradycardie (fréquence cardiaque lente) ou tachycardie (fréquence cardiaque rapide)
- Maux de tête violents
- Appréhension/anxiété/sentiment de malaise
- Changements de vision
- Congestion nasale
- Transpiration
- Peau rougie
- Chair de poule
- Sensation de picotement
SOUS LE NIVEAU DE LESION
- La nausée
- Frissons sans fièvre
- Peau moite
- Sensation de froid
- Pâleur
Les symptômes typiques de la DA chez les enfants sont :
AU-DESSUS DU NIVEAU DE LESION
- Hypertension (augmentation rapide de la pression artérielle, 15 mm Hg systolique plus élevée que d’habitude chez les enfants et 15 à 20 mm Hg systolique plus élevée que d’habitude chez les adolescents)
- Bradycardie (fréquence cardiaque lente) ou tachycardie (fréquence cardiaque rapide)
- Gros mal de tête
- Se sentir nerveux/inquiet/effrayé
- Joues/cou/épaules rouges
- Vue trouble
- Nez encombré
- Transpiration
- Chair de poule
- Fourmillements
SOUS LE NIVEAU DE BLESSURE
- Maux d’estomac, envie de vomir
- Frissons sans fièvre
- Peau moite ou sensation de froid et sueurs
- Sensation de froid
- Pâleur
Dysréflexie autonome silencieuse
Il existe de plus en plus de preuves que certaines personnes ont des épisodes de DA sans symptômes. En d’autres termes, une pression artérielle élevée sans aucune alerte ni symptôme dans le corps. Ces découvertes ont été observées lors de la surveillance de la pression artérielle pendant le sommeil, lors des procédures d’évaluation de la vessie et lors de programmes intestinaux de routine. Dans tous ces cas, la tension artérielle est au niveau du diagnostic/d’élévation de la DA, mais l’individu ne présente aucun symptôme. Il est important que pendant les activités de routine, votre tension artérielle soit surveillée pour repérer une DA. S’il n’y a pas de changement dans votre tension artérielle, une surveillance occasionnelle peut être effectuée. S’il y a des changements dans votre tension artérielle, informez immédiatement votre professionnel de santé pour une évaluation et des instructions supplémentaires.
Diagnostiquer la dysréflexie autonome
La détection de la présence d’une DA se fait par l’évaluation de la pression artérielle. Le plus souvent, un ou plusieurs symptômes sont notés et la pression artérielle doit être mesurée. Les individus ont besoin de connaître leur tension artérielle habituelle, car au fil du temps, avec les troubles neurologiques, en particulier avec les lésions de la moelle épinière, la tension artérielle a tendance à baisser en raison de changements cardiaques causés par un ralentissement de la réponse des vaisseaux sanguins. Les adultes atteints d’une lésion médullaire à T6 et au-dessus peuvent ne pas conserver leur tension artérielle moyenne avant lésion, mais auront souvent une tension artérielle normale pour eux à 90-110 mmg Hg systolique (chiffre supérieur). Vous devez connaître votre tension artérielle normale pour reconnaître une augmentation systolique de 20 à 40 mmg Hg chez les adultes (le chiffre du haut), une augmentation systolique de 15 à 20 mmg Hg chez les adolescents et une augmentation systolique de 15 mmg Hg chez les enfants.
Une dysréflexie autonome sera suspectée chez les individus présentant une lésion des motoneurones supérieurs. L’apparition d’un épisode de DA peut survenir à tout moment chez les personnes atteintes d’une maladie ou d’une blessure neurologique comme un accident vasculaire cérébral, une lésion cérébrale, la sclérose en plaques, le syndrome de Guillain-Barré et autres. Certaines maladies neurologiques sont progressives, donc le temps d’apparition ne peut pas être déterminé car il se produit lorsqu’un individu atteint un point inconnu de la maladie.
Pour les personnes atteintes d’une lésion de la moelle épinière dans la région cervicale ou thoracique, la DA se produit classiquement dans les lésions au-dessus de T6 en raison des effets d’un faisceau de nerfs à T5. Certaines personnes blessées à T10 et au-dessus ont remarqué une DA en raison d’un traumatisme prolongé et de l’anatomie particulière d’un individu. Par le passé, on pensait que la DA ne se produisait pas avant la résolution du choc rachidien (ce qui arrive généralement environ six semaines après le début du traumatisme mais peut parfois prendre plus longtemps). Cependant, des études récentes indiquent que la DA peut survenir au cours du premier mois suivant la blessure. Les personnes atteintes d’une lésion de la moelle épinière dans la région lombaire ou sacrée ont des lésions des nerfs moteurs inférieurs qui ne produisent pas de DA.
Il n’y a pas de test sanguin ou de processus radiologique permettant de détecter la DA, mais les taux de catécholamines et de vasopressine dans le sang peuvent être élevés pendant un épisode de DA ou pendant un certain temps après.
Facteurs déclenchants de la dysréflexie autonome
Classiquement, il a été remarqué que la DA avait un facteur déclenchant qui pousse le corps vers une DA. Un facteur déclenchant est quelque chose que le corps perçoit comme nocif ou irritant en dessous du niveau de lésion. Si le message que quelque chose de petit ou de grand dérange le corps là où la sensation est diminuée, les nerfs sensitifs ne peuvent pas envoyer un message au cerveau pour corriger la situation de manière efficace ou efficiente. En conséquence, le SNA enverrait généralement un message aux nerfs moteurs pour déplacer le corps, ce qui corrigerait la situation. Cependant, en raison d’une mauvaise communication nerveuse, une explosion totale de messages est envoyée. Les messages sont incapables de passer, ce qui entraîne cette explosion massive d’activité nerveuse dans le corps, généralement au-dessus du niveau de lésion.
Avec la découverte de la DA silencieuse, les facteurs déclenchants peuvent ne pas être notés où agir comme un stimulus pour un épisode de DA. Dans la DA silencieuse, la pression artérielle est affectée sans l’identification d’un facteur déclenchant. Un épisode de DA peut survenir sans symptômes, c’est pourquoi on l’appelle DA silencieuse.
Les facteurs déclenchants comprennent une variété de sources nocives ou d’irritations pour le corps. Les élément déclenchants courants sont répertoriés ci-dessous. Les individus ont des éléments déclenchants différents. Les irritations nocives les plus courantes qui stimulent les épisodes de DA proviennent de la vessie, des intestins et de la peau. Cependant, la liste des facteurs déclenchants possibles ne cesse de s’allonger. Ils sont classés en catégories, bien qu’un élément déclenchant pour vous puisse être tout à fait unique.
- La vessie est la principale source documentée de déclenchement d’épisodes de DA. Le plus souvent, la cause est quelque chose qui ne permet pas à l’urine de sortir du corps, ce qui entraîne une distension excessive de la vessie. Cela peut dû à un pli dans un cathéter, à un cathéter bouché, à des spasmes de la vessie, à une dyssynergie du détrusor et du sphincter (DSD, la vessie et le sphincter ne fonctionnant pas à l’unisson), à des calculs, à une infection ou à d’autres contraintes. Pour certains, le cathétérisme intermittent ou les cathéters sus-pubiens peuvent être irritants. Les tests de vessie par cystoscopie (un endoscope inséré dans la vessie), les tests urodynamiques (évaluation de la fonction de la vessie), la lithotritie par ondes de choc (brisant les calculs) peuvent également déclencher la DA. Les équipements utilisés pour la collecte de l’urine, tels que des sangles de sac de jambe trop serrées ou un sac de jambe lourd ou trop plein, des sous-vêtements de collecte d’urine humides ou des sangles de cathéter externes sont également en cause.
- Le deuxième élément déclenchant le plus fréquent de la DA est l’intestin. Une distension intestinale excessive due à un mouvement rapide, un programme intestinal incomplet ou incompétent, une surcharge fécale, une constipation, des gaz, une stimulation digitale régulière ou trop zélée, des lavements ou un retrait manuel sont tous des facteurs déclenchants. La diarrhée ou des problèmes internes tels que la diverticulite, la maladie de Crohn, les fissures et les hémorroïdes peuvent également être des irritants nocifs.
- Les problèmes de peau sont le troisième facteur déclenchant le plus courant de la DA. Les problèmes de peau couvrent un large éventail de démangeaisons qui ne peuvent pas être détectées ou grattées, des éruptions cutanées, des lésions de pression à n’importe quel stade, des coupures, des ecchymoses, des fractures osseuses, des ongles incarnés, des ongles trop longs, le fait d’être assis sur un drap froissé, même juste un courant d’air soufflant sur les poils fins de votre bras ou de votre jambe. Vêtements trop serrés, rugueux ou amples, rivets sur les jeans, chaussures mal ajustées, chaussettes trop serrées aux orteils ou aux jambes, ceintures, soutien-gorge, la liste des problèmes vestimentaires ne cesse de s’allonger.
Au fur et à mesure que de plus en plus de facteurs déclenchants de l’AD sont identifiés, il semble que tout ce qui dérange peut être un problème. Voici quelques éléments déclenchants supplémentaires :
- Changements de température internes tels que fièvre ou frissons, ou externes tels qu’un environnement chaud ou froid
- Spasticité n’importe où dans le corps
- Problèmes internes tels que crises/calculs de la vésicule biliaire, appendicite, problèmes de fonction hépatique, pancréatite, kyste de l’ovaire, prostatite, ulcères du tube digestif, reflux gastrique, etc.
- Thrombose veineuse profonde (TVP) (formation d’un caillot sanguin dans une veine profonde), embolie pulmonaire (EP)
- Ossification hétérotrophe (HO) (présence d’os dans les tissus mous où il ne se trouve généralement pas)
- Hypotension orthostatique (OH) (la pression artérielle chute en position assise ou debout)
- La douleur
- Effets oculaires dus à l’utilisation d’un ordinateur ou au soleil
Traitement de la dysréflexie autonome
La DA est une urgence médicale. Lorsque la pression artérielle est élevée, vous devez agir immédiatement. N’hésitez pas à appeler le 911 si besoin.
- Lorsque les symptômes de la DA sont notés. Commencez par vous asseoir rapidement à la verticale. Votre torse et vos hanches doivent former un angle de 90 degrés. Demandez à quelqu’un de vous aider à vous asseoir si vous ne pouvez pas le faire vous-même. Le passage soudain de la position couchée à la position assise profite de l’hypotension orthostatique lorsque votre tension artérielle chute soudainement, car les vaisseaux sanguins ne peuvent pas se contracter pour faire monter le sang à la tête assez rapidement.
- Continuez à surveiller la tension artérielle toutes les 2-3 minutes jusqu’à ce qu’elle revienne à la normale.
- Desserrez tout ce qui est serré ou restrictif sur votre corps tout en vous mettant en position assise.
- Recherchez la cause de cet épisode de DA. Commencez par vérifier les trois facteurs déclenchants les plus courants de la DA. Vérifiez le débit urinaire. Cathétérisez si nécessaire (s’il n’y a pas ou peu de diurèse). Ensuite, vérifiez s’il y a un blocage de l’intestin. Désimpactez l’intestin si des selles sont présentes. Ensuite, vérifiez la peau en éliminant les plis, les constrictions ou les vêtements serrés. Vous connaissez peut-être vos facteurs déclenchants des épisodes de DA précédents. La correction de votre source de déclenchement habituelle est un bon début si vous en êtes conscient. Si la DA ne commence pas à se résoudre avec des corrections, continuez à rechercher et à supprimer les éléments déclenchants en dessous du niveau de la blessure.
- Si vous avez un médicament prescrit pour la DA, administrez-le. Le médicament peut consister en un antihypertenseur d’action rapide et de courte durée. Les médicaments couramment prescrits sont :
- Nitro Paste—1/2″ (pour les personnes de moins de 13 ans) ou 1″ (pour les personnes de 13 ans et plus), appliquer toutes les 30 minutes, localement au-dessus du niveau de blessure. Réappliquez si nécessaire. Laver la pâte Nitro lorsque la pression artérielle est stable pour éviter de trop faire baisser la pression artérielle.
- Nifédipine (si la pâte Nitro n’est PAS disponible) – 0,25-0,5 mg/kg par dose (pour les personnes de moins de 13 ans) ou 10 mg par dose (pour les personnes de 13 ans et plus), injectez la forme à libération immédiate par voie sublinguale (sous la langue) ou s’il est sous forme de pilule, mâchez-la. Cela peut être répété toutes les 20 à 30 minutes au besoin.
- Les antihypertenseurs IV ne peuvent être administrés qu’en milieu surveillé (soins intensifs) car une surveillance étroite est requise.
- D’autres médicaments utilisés pour traiter les épisodes de DA en cours et dangereux comprennent la nifédipine, les nitrates, le captopril, la térazosine, la prazosine, la phénoxybenzamine, la prostaglandine ED et le sildénafil. Le choix du médicament qui vous convient doit être fait en consultation avec votre professionnel de la santé.
- Votre tension artérielle devrait commencer à baisser et à se corriger. Continuez à surveiller votre tension artérielle pendant au moins deux heures
- Si le ou les facteurs déclenchants sont détectés et supprimés ou corrigés mais que la pression artérielle reste élevée, appelez le 911. Des soins médicaux sont nécessaires immédiatement pour prévenir un événement cardiovasculaire tel qu’un accident vasculaire cérébral, un arrêt cardiaque, des convulsions, une hémorragie rétinienne, un œdème pulmonaire et la mort.
Si vous avez identifié des facteurs déclenchants spécifiques de la DA, d’autres médicaments et des traitements peuvent être utilisés pour aider à contrôler ces causes connues. Cela peut inclure des médicaments pour une dyssynergie du sphincter du détrusor (DSD), une sphinctérotomie (un petit élargissement du sphincter urinaire d’un homme pour résoudre l’augmentation de la pression vésicale), un changement de type de cathéter utilisé ou l’ajout d’un médicament anesthésiant lors de l’insertion du cathéter.
Des modifications du régime alimentaire pour la consistance des selles, l’utilisation d’une approche douce de la stimulation digitale ou par suppositoire, ou une anesthésie locale pour les programmes intestinaux aideront si les problèmes intestinaux sont des facteurs déclenchants de la DA.
Pour aider à réduire les facteurs déclenchants cutanés, des médicaments peuvent être utilisés pour contrôler le tonus (spasmes). Il convient aussi de s’assurer que vous n’êtes pas assis sur un pli ou qu’il n’y a pas un autre irritant cutané, d’effectuer des relâchements de pression et de vérifier que votre peau n’est pas blessée par pression, et il peut falloir utiliser un dissipateur de pression. Surveillez votre sac de jambe si vous en utilisez un pour vous assurer qu’il ne tire pas sur votre jambe parce qu’il se remplit d’urine, vérifiez vos chaussures pour vous assurer qu’elles sont bien ajustées et gardez une bonne hygiène des pieds en évitant les callosités fissurées et les ongles incarnés. Soyez prudent avec votre corps lorsque vous vous déplacez pour éviter les blessures. Protégez vos yeux de la surutilisation de l’ordinateur et de l’exposition au plein soleil.
Vidéo sur la dysréflexie autonome
Une vidéo expliquant la cause et les traitements de la dysréflexie autonome de la Fondation Reeve peut être visionnée ici.
Carte portefeuille sur la dysréflexie autonome
Pour vous assurer d’avoir des informations à jour sur la dysréflexie autonome (DA), téléchargez la carte portefeuille sur la dysréflexie autonome du Christopher & Dana Reeve Foundation National Paralysis Resource Center. Cette carte peut être partagée avec les professionnels de la santé, les soignants, les enseignants et autres. La carte portefeuille est une carte à trois volets facile à transporter qui peut être placée dans votre portefeuille pour un accès rapide. Elle est disponible pour les adultes et les enfants ainsi que dans une variété de langues. Téléchargez la carte de portefeuille AD à partir de : https://www.christopherreeve.org/fr/international/french-hub/cartes-portefeuille ou appelez les spécialistes de l’information Reeve pour obtenir une copie imprimée gratuite au 800-539-7309.
Réhabilitation pour la dysréflexie autonome
Vous devrez participer à l’identification des épisodes de DA. Dès que vous commencez à ressentir un épisode de DA, commencez le traitement en vous asseyant. Appelez à l’aide pour être sûr de ne pas tomber, de ne pas vous blesser ou de ne pas perdre connaissance. Quelqu’un doit appeler le 911 si le facteur déclenchant ne peut pas être identifié ou si les tentatives de traitement ne fonctionnent pas.
Un physiatre, un neurologue, un médecin traitant, un médecin ou une infirmière praticienne qui peut diagnostiquer la DA fournira des traitements adaptés à vos épisodes de DA. Si les épisodes sont facilement corrigés, une surveillance avec une attention particulière pour éviter les éléments déclenchants identifiés peut être nécessaire. Dans les cas plus graves, des médicaments pour traiter la DA seront prescrits. De plus, si votre facteur déclenchant est connu, des médicaments peuvent être prescrits pour l’atténuer, permettant ainsi de réduire ou d’éliminer les épisodes de DA.
Une infirmière autorisée en réadaptation fait partie du personnel soignant qui peut vous renseigner sur la DA à l’hôpital, à l’hôpital de réadaptation ou dans la communauté. Elle peut vous aider à apprendre à l’identifier et à la traiter, et aussi vous apprendre à faire face aux situations d’urgence.
Un urologue peut fournir un traitement tel que des agents anesthésiants de la vessie et des traitements pour éviter de déclencher la DA.
Les prestataires de soins à domicile peuvent vous aider à surveiller les épisodes de DA et à fournir des soins d’urgence. Ce sont généralement eux qui appellent le 911, au besoin. Si vous êtes atteint de DA, vous devez informer tous vos fournisseurs de soins de santé et vos soignants de votre état au cas où un épisode se produirait, et que vous n’ayez pas le temps d’appeler à l’aide. Cela inclut les thérapeutes qui fourniront une thérapie en utilisant des stratégies pour éviter un épisode de DA et tous les soignants qui peuvent assurer votre sécurité.
Recherche
Traditionnellement, la recherche sur les causes et les traitements de la dysréflexie autonome s’est concentrée sur le facteur déclenchant individuel tel que le tonus (spasmes), la pression, la vessie et les problèmes intestinaux. Cependant, les professionnels de la santé notent que les personnes qui sont traitées pour un tonus ou une douleur neuropathique ont moins d’incidence de DA. Cela a suscité un intérêt pour une meilleure compréhension du système nerveux autonome dans son ensemble en vue de traitements plutôt que pour un seul sous-ensemble de causes (Rabchevsky, et al., 2011).
Une étude des tests du système nerveux autonome a été conduit pour voir si les causes prédictives de la DA pouvaient être isolées. La respiration profonde, la manœuvre de Valsalva et le test de la table inclinable sont des tests auxquels ont été soumises des personnes atteintes de lésions de la moelle épinière. Les mesures de la sensibilité baroréflexe (BRS) et l’analyse spectrale de la variabilité de la fréquence cardiaque et de la pression artérielle ont été évaluées ainsi que les taux sanguins de catécholamines et de vasopressine et des examens cliniques et radiologiques. Une DA a été démontrée chez 73,3 % des patients atteins de lésions de la moelle épinière, 63,6 % d’entre eux étaient asymptomatiques (CívicosSánchez, et al., 2021). Bien que cette étude ne soit pas pratique en utilisation clinique à l’heure actuelle, il s’agit d’une évaluation efficace des personnes atteintes de la DA permettant peut-être d’identifier des personnes qui ne présentent aucun symptôme.
La DA silencieuse a récemment été mise au premier plan des soins pour les personnes souffrant de perturbation du SNA. Auparavant, on pensait que la DA était uniquement présente chez les individus présentant des symptômes. Récemment, des scientifiques ont découvert la DA chez des individus qui ne présentaient aucun symptôme. Cela se manifeste par une pression artérielle élevée, mais aucun changement dans le confort corporel. La DA silencieuse est désormais un problème critique pour les personnes à risque de complications graves mais sans signe avant coureur (Kirshblum, et al., 2002 ;Linsenmeyer, et al., 1996.)
La recherche chez la souris démontre que la DA à d’autres effets sur le fonctionnement du système immunitaire. Une étude de suivi d’un individu a noté une libération excessive de catécholamines affectant le système immunitaire, ce qui indique que la DA peut être une cause secondaire de déficit immunitaire après une LME (Zhang, et al., 2013). Cette nouvelle information nécessitera une étude plus approfondie car la SCI a un effet sur la diminution du fonctionnement immunitaire. En plus de la neuro inflammation du système nerveux, d’autres effets de la DA sur le système immunitaire sont à l’étude avec des traitements encore à définir (Mironets, et al., 2018)
Faits et chiffres
Les personnes atteintes d’une lésion médullaire au niveau T6 ou supérieur ont un taux de DA de 48 à 90 %.
La DA silencieuse est présente chez les personnes atteintes d’une LME au niveau T6 ou supérieur à un taux de 42,9 à 63,6 %.
Le taux de DA chez les enfants de 13 ans et plus jeunes atteints d’une lésion de la moelle épinière à T6 ou au-delà dans une étude à site unique était de 51 %.
Le taux de mortalité avec DA est de 22 % et le risque d’AVC augmente de 300 % à 400 %.
La dysréflexie autonome survient plus souvent chez les personnes ayant une classification complète de la moelle épinière à 91 %, que chez ceux ayant une classification incomplète à 27 %. Le temps d’apparition de la DA est plus court pour ceux dont la classification médullaire est complète et plus long pour ceux dont la classification est incomplète.
Incidence du dysfonctionnement autonome dans les traumatismes cérébraux dans une étude de 349 cas rapportés :
- Traumatisme cérébral (TCC) 79,4 %
- Hypoxie 9,7%
- Accident vasculaire cérébral ou accident vasculaire cérébral 5,4 %
Ressources au consommateur
Si vous cherchez plus d’informations sur les lésions de la moelle épinière ou si vous avez une question spécifique, nos spécialistes de l’information sont disponibles les jours ouvrables, du lundi au vendredi, au 800-539-7309 (numéro sans frais aux États-Unis) de 7h à 00h (heure de l’Est aux États-Unis).
Directives cliniques :
Consortium pour la médecine des lésions de la moelle épinière. Prise en charge aiguë de la dysréflexie autonome : personnes atteintes d’une lésion de la moelle épinière se présentant dans des établissements de soins de santé 2e édition. © Copyright 2001, Vétérans paralysés d’Amérique. https://pva-cdnendpoint.azureedge.net/prod/libraries/media/pva/library/publications/cpg_autonomic-dysreflexia.pdf
Washington State Department of Health, Office of Community Health Systems Emergency Medical Services & Trauma Section Trauma Rehabilitation Clinical Guideline Autonomic Dysreflexia, 15 janvier 2020. https://www.doh.wa.gov/Portals/1/Documents/Pubs/530237.pdf
Références
Baguley IJ, Perkes IE, Fernandez-Ortega JF, Rabinstein AA, Dolce G, Hendricks HT; Consensus Working Group. Paroxysmal sympathetic hyperactivity after acquired brain injury: consensus on conceptual definition, nomenclature, and diagnostic criteria. J Neurotrauma. 2014 Sep 1;31(17):1515-20. doi: 10.1089/neu.2013.3301. Epub 2014 Jul 28. PMID: 24731076.
Canon S, Shera A, Phan NM, Lapicz L, Scheidweiler T, Batchelor L, Swearingen C. Autonomic dysreflexia during urodynamics in children and adolescents with spinal cord injury or severe neurologic disease. J Pediatr Urol. 2015 Feb;11(1):32.e1-4. doi: 10.1016/j.jpurol.2014.08.011. Epub 2014 Oct 8. PMID: 25697979.
Caruso D, Gater D, Harnish C. Prevention of recurrent autonomic dysreflexia: a survey of current practice. Clin Auton Res. 2015 Oct;25(5):293-300. doi: 10.1007/s10286-015-0303-0. Epub 2015 Aug 18. PMID: 26280219.
Cívicos Sánchez N, Acera M, Murueta-Goyena A, Sagastibeltza N, Martínez R, Cuadrado M, Orueta A, Tijero B, Fernández T, Del Pino R, Gabilondo I, Jauregui Abrisqueta ML, Gómez Esteban JC. Quantitative analysis of dysautonomia in patients with autonomic dysreflexia. J Neurol. 2021 Aug;268(8):2985-2994. doi: 10.1007/s00415-021-10478-w. Epub 2021 Feb 25. PMID: 33634338.
Cowan H, Lakra C, Desai M, Autonomic dysreflexia in spinal cord injury. BMJ 2020;371:m3596. doi: https://doi.org/10.1136/bmj.m3596.
Ekland MB, Krassioukov AV, McBride KE, Elliott SL. Incidence of autonomic dysreflexia and silent autonomic dysreflexia in men with spinal cord injury undergoing sperm retrieval: implications for clinical practice. J Spinal Cord Med. 2008;31(1):33-9. doi: 10.1080/10790268.2008.11753978. PMID: 18533409; PMCID: PMC2435024.
Eldahan KC, Rabchevsky AG. Autonomic dysreflexia after spinal cord injury: Systemic pathophysiology and methods of management. Auton Neurosci. 2018 Jan;209:59-70. doi: 10.1016/j.autneu.2017.05.002. Epub 2017 May 8. PMID: 28506502; PMCID: PMC5677594.
Giannantoni A, Di Stasi SM, Scivoletto G, Mollo A, Silecchia A, Fuoco U, Vespasiani G. Autonomic dysreflexia during urodynamics. Spinal Cord. 1998 Nov;36(11):756-60. doi: 10.1038/sj.sc.3100684. PMID: 9848482.
Helkowski WM, Ditunno JF Jr, Boninger M. Autonomic dysreflexia: incidence in persons with neurologically complete and incomplete tetraplegia. J Spinal Cord Med. 2003 Fall;26(3):244-7. doi: 10.1080/10790268.2003.11753691. PMID: 14997966.
Hickey KJ, Vogel LC, Willis KM, Anderson CJ. Prevalence and etiology of autonomic dysreflexia in children with spinal cord injuries. J Spinal Cord Med. 2004;27 Suppl 1:S54-60. doi: 10.1080/10790268.2004.11753786. PMID: 15503704.
Huang YH, Bih LI, Liao JM, Chen SL, Chou LW, Lin PH. Blood pressure and age associated with silent autonomic dysreflexia during urodynamic examinations in patients with spinal cord injury. Spinal Cord. 2013 May;51(5):401-5. doi: 10.1038/sc.2012.155. Epub 2012 Dec 11. PMID: 23229618.
Karlsson AK. Autonomic dysreflexia. Spinal Cord. 1999 Jun;37(6):383-91. doi: 10.1038/sj.sc.3100867. PMID: 10432257.
Kirshblum SC, House JG, O’connor KC. Silent autonomic dysreflexia during a routine bowel program in persons with traumatic spinal cord injury: a preliminary study. Arch Phys Med Rehabil. 2002 Dec;83(12):1774-6. doi: 10.1053/apmr.2002.36070. PMID: 12474185.
Krassioukov AV, Furlan JC, Fehlings MG. Autonomic dysreflexia in acute spinal cord injury: an under-recognized clinical entity. J Neurotrauma. 2003 Aug;20(8):707-16. doi: 10.1089/089771503767869944. PMID: 12965050.
Krassioukov A, Warburton DE, Teasell R, Eng JJ; Spinal Cord Injury Rehabilitation Evidence Research Team. A systematic review of the management of autonomic dysreflexia after spinal cord injury. Arch Phys Med Rehabil. 2009 Apr;90(4):682-95. doi: 10.1016/j.apmr.2008.10.017. PMID: 19345787; PMCID: PMC3108991.
Lee ES, Joo MC. Prevalence of autonomic dysreflexia in patients with spinal cord injury above T6. Biomed Res Int. 2017;2017:2027594. doi: 10.1155/2017/2027594. Epub 2017 Oct 26. PMID: 29226126; PMCID: PMC5684522.
Linsenmeyer TA, Campagnolo DI, Chou IH. Silent autonomic dysreflexia during voiding in men with spinal cord injuries. J Urol. 1996 Feb;155(2):519-22. PMID: 8558650.
Liu N, Zhou M, Biering-Sørensen F, Krassioukov AV. Iatrogenic urological triggers of autonomic dysreflexia: a systematic review. Spinal Cord. 2015 Jul;53(7):500-9. doi: 10.1038/sc.2015.39. Epub 2015 Mar 24. PMID: 25800696.
Meyfroidt G, Baguley IJ, Menon DK. Paroxysmal sympathetic hyperactivity: the storm after acute brain injury. Lancet Neurol. 2017 Sep;16(9):721-729. doi: 10.1016/S1474-4422(17)30259-4. Erratum in: Lancet Neurol. 2018 Mar;17 (3):203. PMID: 28816118.
Mironets E, Osei-Owusu P, Bracchi-Ricard V, Fischer R, Owens EA, Ricard J, Wu D, Saltos T, Collyer E, Hou S, Bethea JR, Tom VJ. Soluble TNFα Signaling within the spinal cord contributes to the development of autonomic dysreflexia and ensuing vascular and immune dysfunction after spinal cord injury. J Neurosci. 2018 Apr 25;38(17):4146-4162. doi: 10.1523/JNEUROSCI.2376-17.2018. Epub 2018 Apr 2. PMID: 29610439; PMCID: PMC5963850.
Naftchi NE, Richardson JS. Autonomic dysreflexia: pharmacological management of hypertensive crises in spinal cord injured patients. J Spinal Cord Med. 1997 Jul;20(3):355-60. PMID: 9261783.
Perkes I, Baguley IJ, Nott MT, Menon DK. A review of paroxysmal sympathetic hyperactivity after acquired brain injury. Ann Neurol. 2010 Aug;68(2):126-35. doi: 10.1002/ana.22066. PMID: 20695005.
Perrouin-Verbe B, Courtois F, Charvier K, Giuliano F. Sexualité de la patiente neurologique [Sexuality of women with neurologic disorders]. Prog Urol. 2013 Jul;23(9):594-600. French. doi: 10.1016/j.purol.2013.01.004. Epub 2013 Mar 7. PMID: 23830253.
Rabchevsky AG, Kitzman PH. Latest approaches for the treatment of spasticity and autonomic dysreflexia in chronic spinal cord injury. Neurotherapeutics. 2011 Apr;8(2):274-82. doi: 10.1007/s13311-011-0025-5. PMID: 21384222; PMCID: PMC3101828.
Teasell RW, Arnold JM, Krassioukov A, Delaney GA. Cardiovascular consequences of loss of supraspinal control of the sympathetic nervous system after spinal cord injury. Arch Phys Med Rehabil. 2000 Apr;81(4):506-16. doi: 10.1053/mr.2000.3848. PMID: 10768544.
Weaver LC, Marsh DR, Gris D, Brown A, Dekaban GA. Autonomic dysreflexia after spinal cord injury: central mechanisms and strategies for prevention. Prog Brain Res. 2006;152:245-63. doi: 10.1016/S0079-6123(05)52016-8. PMID: 16198705.
Zhang Y, Guan Z, Reader B, Shawler T, Mandrekar-Colucci S, Huang K, Weil Z, Bratasz A, Wells J, Powell ND, Sheridan JF, Whitacre CC, Rabchevsky AG, Nash MS, Popovich PG. Autonomic dysreflexia causes chronic immune suppression after spinal cord injury. J Neurosci. 2013 Aug 7;33(32):12970-81. doi: 10.1523/JNEUROSCI.1974-13.2013. PMID: 23926252; PMCID: PMC3735880.

